
Analytische Techniken, die auf Lichtstreuung basieren, sind für die Quantifizierung von Qualitätsmerkmalen und anderen Eigenschaften von Gentherapeutika unerlässlich. Dynamische Lichtstreuung (DLS) und Mehrwinkel-Lichtstreuung (MALS) gekoppelt an Trenntechnologien (SEC-MALS, FFF-MALS) geben Aufschluss über molare Masse und Größe, Aggregation, physikalischen Titer, Leer:Voll-Verhältnis und Stabilität.
Im Folgenden werden die von Wyatt angebotenen Lösungen für Anforderungen der Industrie und der Behörden an AAVs und andere DNA/RNA-Therapeutika vorgestellt. Lichtstreutechniken sind einfach zu bedienen und erhöhen die Produktivität, während sie direkt Auskunft über die zentralen, kritischen, biophysikalischen Eigenschaften geben, die auch als critical quality attributes (CQAs) definiert werden.
Größe, Stabilität und Titer im Hochdurchsatz bestimmen
Die Dynamische Lichtstreuung (DLS) ermöglicht schnelle, nicht-destuktive Messungen bei geringem Probenverbrauch für eine Vielzahl von Trägermedien, einschließlich AAVs (Adeno-assoziierte Viren), Lentiviren und Lipid-Nanopartikeln. Der
DynaPro™ Plate Reader ist das führende Werkzeug für die Hochdurchsatz-Bestimmung von Produktqualität, -stabilität und -quantität, direkt in Mikrotiterplatten. Der
DynaPro™ NanoStar™ ermöglicht die gleichen Messungen in einer Quarzküvette mit Volumina von nur 2 µL. Unser White Paper WP5003: Automated dynamic and static light scattering in microwell plates for fast, productive development of biologics zeigt die wichtigsten Aspekte von DLS für die Analyse vieler Klassen von Biotherapeutika.

Quantifizierung von viralen Vektoren
Die direkte Messung der gesamten Viruspartikelkonzentration kann in wenigen Sekunden mit dem DynaPro Plate Reader oder dem NanoStar durchgeführt werden. Die durch DLS gemessene hydrodynamische Größe wird mit der gleichzeitigen Intensitätsmessung durch statische Lichtstreuung (SLS) kombiniert, um genaue Partikelkonzentrationen zu bestimmen. Die Technik eignet sich sowohl für kleine virale Vektoren, wie AAVs, als auch für größere Viren und Lipid-Nanopartikel.
DLS-Messungen von drei AAV-Proben, S1, S2 und S3, zeigen, dass eine davon (S3) einen kleinen Anteil großer Aggregate mit Radius >100 nm enthält. Diese Aggregatpopulation wird detektiert und quantifiziert, obwohl ihre Konzentration einen kleinen Bruchteil der gesamten Partikelanzahl ausmacht. Die Partikelkonzentration in den DynaPro-Geräten stimmt gut mit anderen quantitativen Techniken überein, einschließlich SEC-MALS (mehr Details unten). Wichtig ist, dass die Chargencharakterisierung mit DLS die Erkennung und Quantifizierung größerer Spezies ermöglicht, die unter Chromatographiebedingungen entfernt oder gestört werden können.
Details finden Sie in der Application Note AN5007: Characterization of AAV-based viral vectors by DynaPro DLS/SLS instruments.
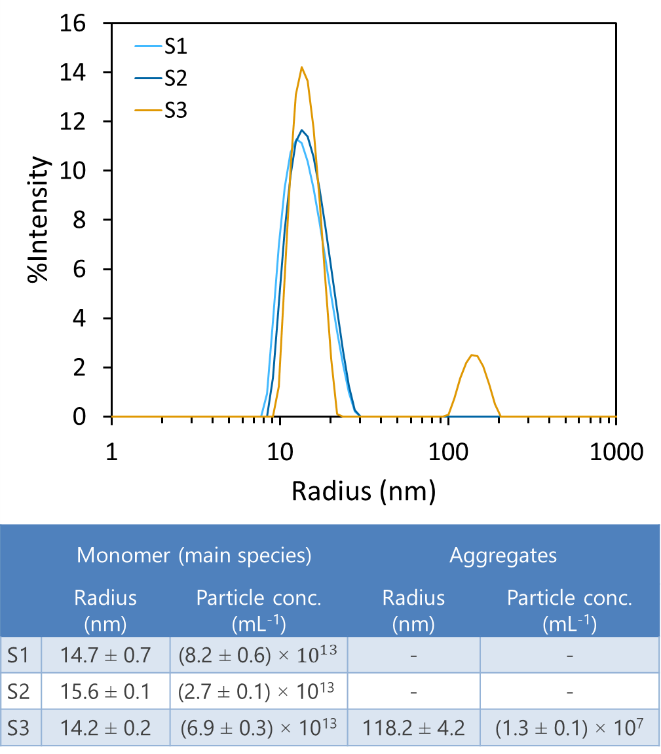
DLS-Analyse von drei AAV-Proben mit Angabe der Größe und Konzentration. S3 weist eine Population von großen Aggregaten auf.
Formulation screening
Die Möglichkeit, Gentherapieformulierungen in frühen Entwicklungsstadien zu screenen, stellt sicher, dass nur die am besten geeigneten Kandidaten weiterführend untersucht werden. Die Messung der Größe und Größenverteilungen mit DLS ermöglicht eine schnelle Beurteilung des Aggregationsgrades und der Stabilität einer Probe.
Mit den zur Verfügung stehenden Analyse- und Visualisierungswerkzeugen, die die DYNAMICS™-Software bietet, können Wissenschaftler auf einfache Weise mehrere Qualitätsattribute bestimmen, um ein möglichst stabiles und robustes Produkt zu entwickeln. Zu diesen Analysen gehören die folgenden:
- Screening der Größe und Größenverteilung mit Beurteilung des Aggregatgehaltes
- Identifizierung der mobilen SEC-Phasen oder von Formulierungspuffern, die eine gute Produktqualität fördern
- Messung der kolloidalen Stabilität und der Neigung zur Aggregation
- Bestimmung der Konformationsstabilität anhand der Aggregationstemperatur oder der Zeit bis zur Aggregation
Erfahren Sie im Webinar “Quantification of viral and non-viral vector CQAs” mehr über die Anwendung der DLS-Werkzeuge von Wyatt für das High-throughput Screening.

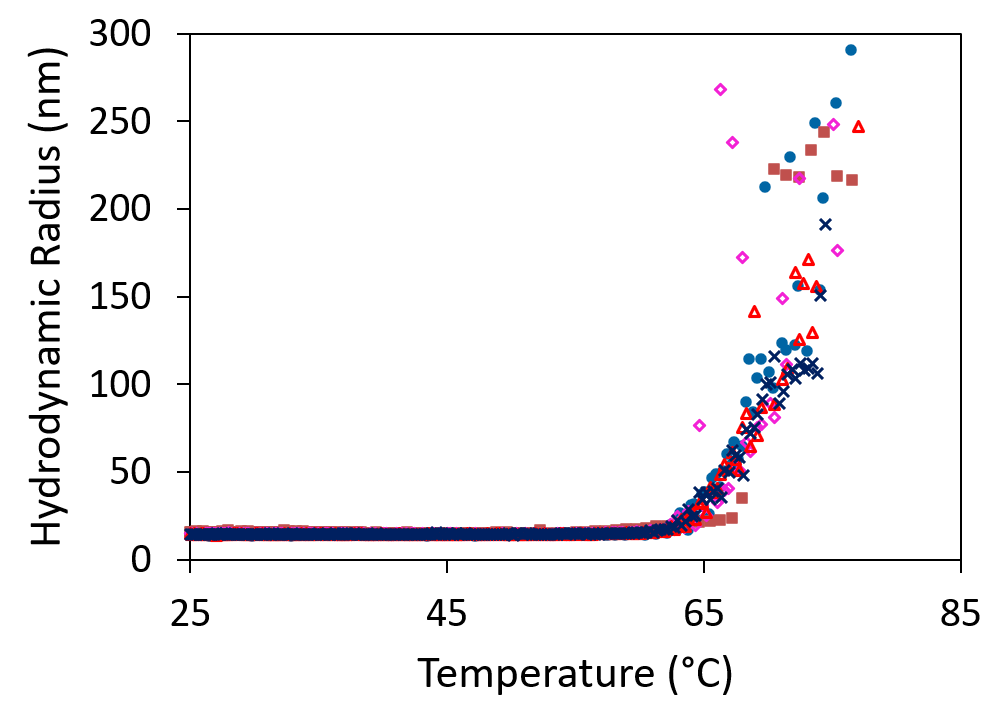
Das Screening von Biologika-Formulierungen in einer Mikrotiterplatte liefert schnelle Hinweise auf die Aggregation (oben) und die Temperatur des Aggregationsbeginns (unten).
Qualität und Quantität von AAVs und assoziierten Proteinen
Die Größenausschlusschromatographie (SEC) in Kombination mit der Mehrwinkel-Lichtstreuung (MALS) ist ideal geeignet für die Trennung, Charakterisierung, Quantifizierung und Beurteilung des Nukleinsäuregehalts von Gentherapie-Vektoren und artverwandter Proteine. Diese Methode verwendet einen DAWN™MALS-Detektor in Kombination mit einem Optilab™-Detektor zur Bestimmung des differentiellen Brechungsindex (dRI) und einem HPLC-UV-Modul zur Messung der absoluten molaren Masse, Größe und Konzentration von Proteinen, Nukleinsäuren und biologischen Nanopartikeln.
Für die vollständige Charakterisierung von kleinen Proteinen und Nukleinsäuren steht eine große Auswahl an Wyatt-Säulen zur Verfügung. Die Säulengrößen reichen von weniger als ein paar kDa bis hin zu kleinen Viren, typischerweise mit einem Durchmesser von 50 nm. Weitere Informationen finden Sie in unserem Accessories & Services Guide.

Ein komplettes SEC-MALS-System umfasst den DAWN-MALS-Detektor, den Optilab dRI-Detektor und dem Industriestandard entsprechende HPLC-Pumpen, Autosampler und UV-Detektoren.
Molmassen- und Größenverteilungen
Molmassen- und Größenmessungen mit SEC-MALS sind nicht auf Proteine beschränkt. Kurze Oligonukleotide, Polysaccharide, ganze Plasmide und kleine Bionanopartikel können mit SEC-MALS vollständig charakterisiert werden. Diese Technik liefert unschätzbare Informationen über die Homogenität Ihrer Proben, den Grad der Konjugation und Aggregation.
Hier zeigen wir die gemessene molare Masse für zwei Plasmide, eines mit 12 kbp und das andere mit 6 kbp. Die gleichmäßige Molmassenverteilung über den Peak stimmt gut mit den erwarteten Sequenzergebnissen überein. Der Anstieg des RMS-Radius an der Vorderkante des Peaks kann auf eine geringe Anzahl von Aggregaten hindeuten oder auf die Koelution von linearer oder "nicked" Konformation mit gleicher molaren Masse aber größerem Radius.
Der Bereich der Charakterisierung ist nur durch den Trennbereich der SEC-Säule begrenzt. MALS-Messungen für größere Viren und Nanopartikel sind mit FFF-MALS (siehe unten) leicht zu erreichen. Erfahren Sie mehr über SEC-MALS in WP1615: SEC-MALS for absolute biophysical characterization.
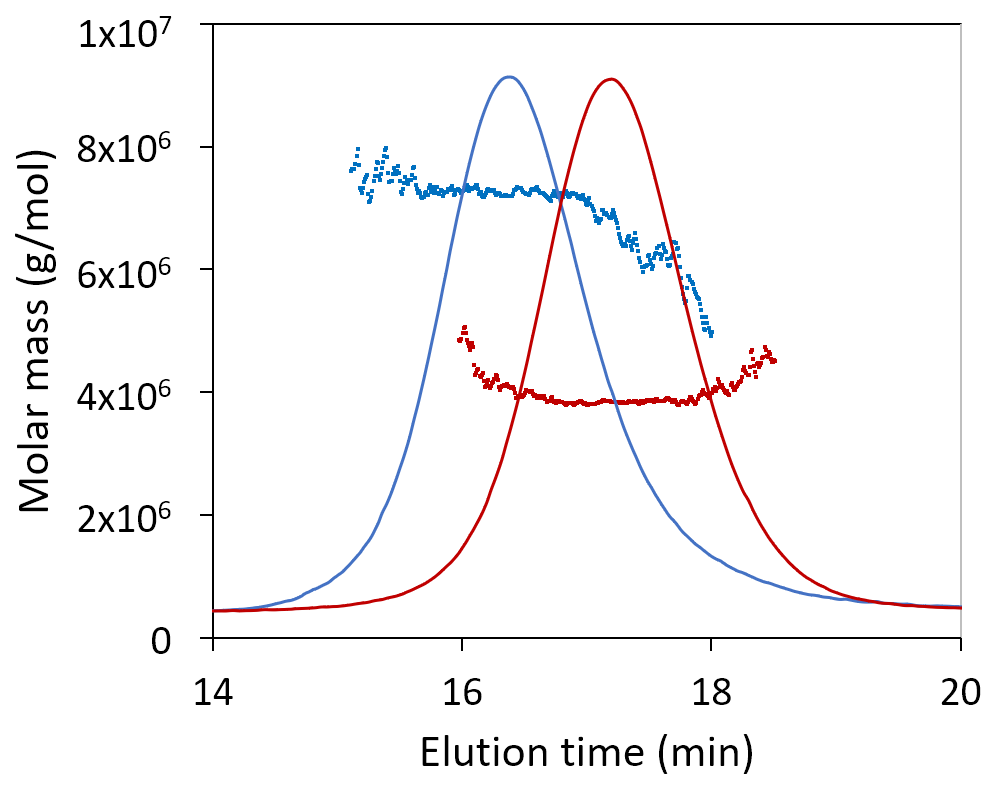
SEC-MALS-Analyse von 6 kbp- und 12 kbp-Plasmiden zur Bestimmung ihrer molaren Massen und Radien. Zunehmende Größe bei konstanter Molmasse (blau) kann ein Hinweis auf Aggregate oder auf Monomere mit gestreckter Konformation sein.
AAV Critical Quality Attributes
Um eine sichere und wirksame Gentherapie mit einem Adeno-assoziierten Virus als Verabreichungsvektor zu gewährleisten, muss das Produkt eine Reihe von Qualitätsmerkmalen erfüllen, darunter Konzentration und Gehalt.
Die Gesamtpartikelkonzentration, die direkt mit der Dosierung zusammenhängt, ist von entscheidender Bedeutung. SEC-MALS ist in einzigartiger Weise für die Messung der Gesamtpartikelkonzentration dieser kleinen viralen Vektoren geeignet; die Ergebnisse sind robust und zuverlässig über alle Serotypen hinweg, ohne dass Primer aufwendig designt werden müssen oder eine komplexe Probenvorbereitung erforderlich sind. Die SEC-MALS-Analyse des Kapsidgehalts bestimmt die Anzahl der vollen und leeren Virionen.
Die in die ASTRA™-Software integrierte Virale-Vektor-Analyse ermöglicht die direkte Messung der Gesamtpartikelkonzentration (Kapsid) und des Kapsidgehalts. Die Ergebnisse von SEC-MALS sind mit denen anderer Techniken vergleichbar und können zur Validierung von PCR- oder ELISA-Assays verwendet werden. Neben dem Anteil an vollen und leeren Kapsiden bestimmt SEC-MALS auch die molaren Massen der Protein- und Nukleinsäureanteile. Kombiniert mit ASTRAs 21CFR11 konformen Version ist SEC-MALS leicht für lot-to-lot-Vergleiche oder Freigabe-Assays von Gentherapieprodukten einsetzbar.
Erfahren Sie mehr über diese Messungen in unserer Application Note AN1617: Quantifying quality attributes of AAV gene therapy vectors by SEC-UV-MALS-dRI.
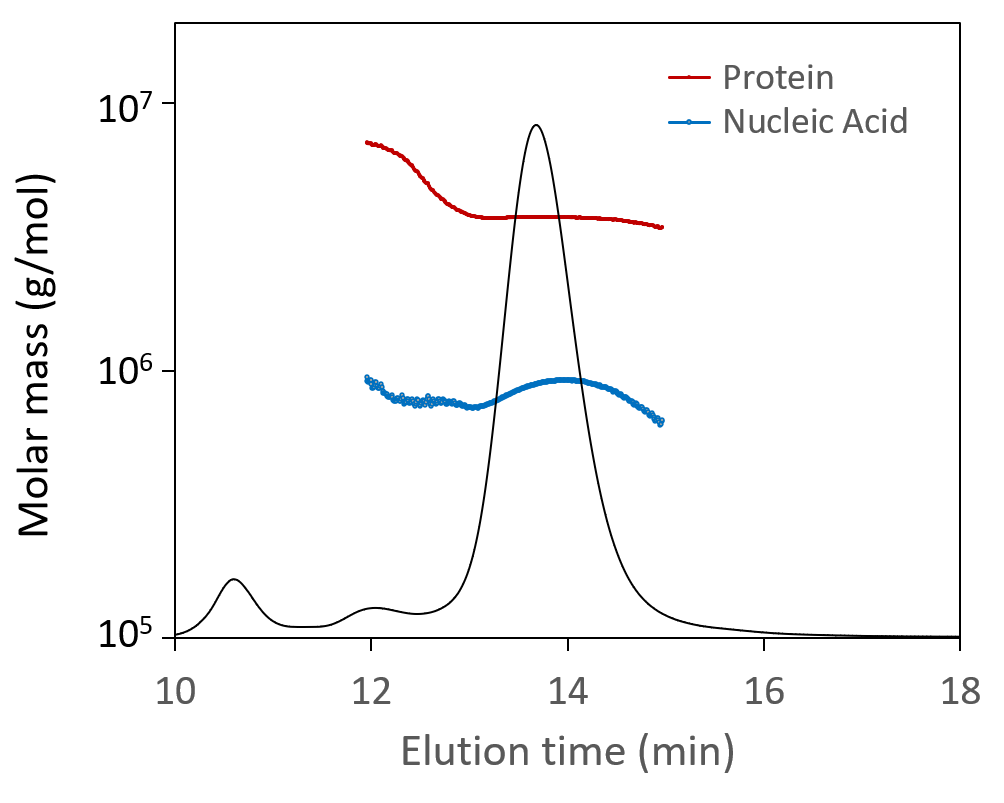
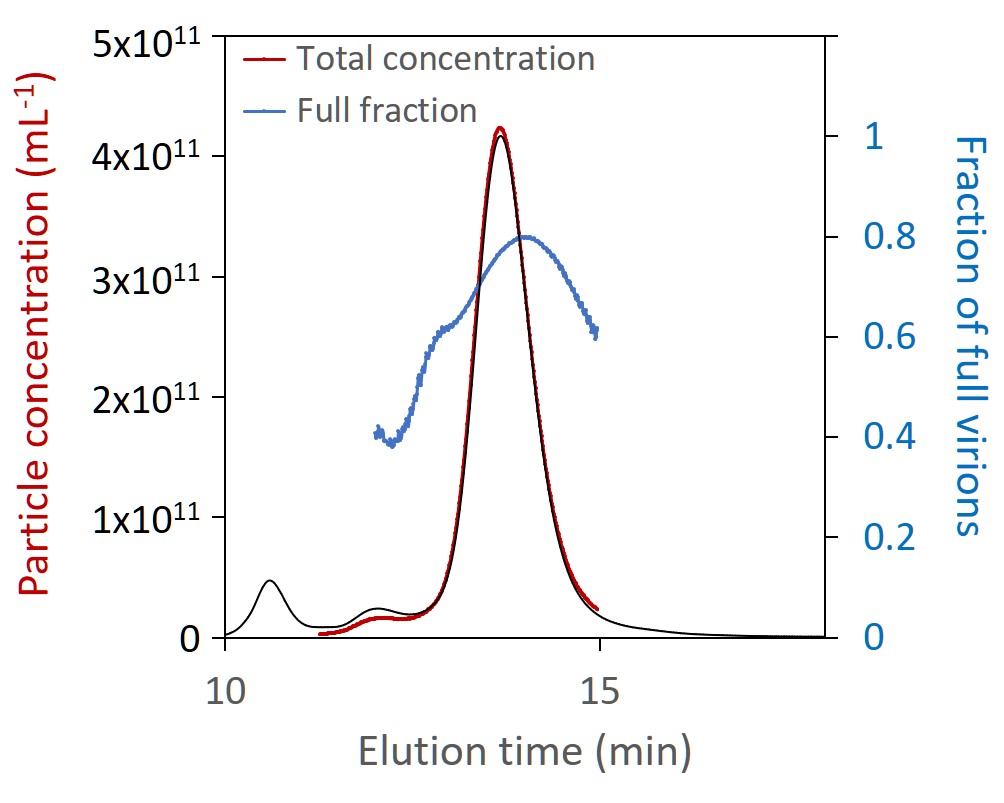
Die SEC-MALS-Analyse von AAV-CQAs liefert gleichzeitig die molare Masse von Kapsiden und Nukleinsäuren (oben) sowie die Gesamtkapsidkonzentration und den Anteil der vollen Kapside (unten). Beide Ergebnisse in der Darstellung überlagert mit Lichtstreuchromatogrammen.
Aggregate, große Viren und mRNA
Während SEC-MALS Qualitätsattribute über einen breiten Größenbereich misst, ist die Technik in Bezug auf größere Partikel und Aggregate limitiert. Dies liegt daran, dass SEC-Säulen diese Spezies entfernen oder scheren können, was zu einer unvollständigen Charakterisierung und Quantifizierung führt.
Die Feldflussfraktionierung (FFF) mit dem Eclipse™ FFF-System bietet eine schonende Trennung in einem offenen Kanal ohne stationäre Phase. Dadurch wird die Möglichkeit beseitigt, dass die Probe abgebaut oder durch die Trennmatrix entfernt wird. FFF in Verbindung mit MALS liefert genaue Größen, molare Massen und Partikelkonzentrationen für Bionanopartikel mit einem Durchmesser von bis zu ~1 µm. Wie auf der Seite Lösungen für die Charakterisierung von Lipid-Nanopartikeln erwähnt, kann FFF-MALS auch die Verkapselungseffizienz und den Beladungsgrad von nicht-viralen Vektoren bestimmen.
Laden Sie unsere Publikationsliste herunter, um Beispiele für die Anwendung von FFF-MALS bei der Charakterisierung von Nano-Wirkstoffträgern zu erhalten.
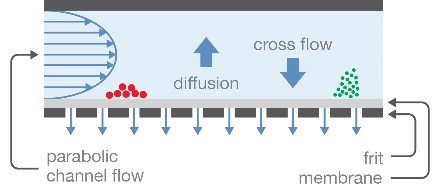
Die Feldflussfraktionierung trennt Partikel nach ihrem hydrodynamischen Radius in einem offenen Kanal.
Charakterisierung über einen weiten Bereich von Partikelgrößen
Lentiviren, Lipid-Nanopartikel und mRNA sind oft zu groß, um von einer SEC-Säule zu eluieren. In diesem Fall ist FFF-MALS ideal für die Trennung und Charakterisierung.
Bei der Analyse mittels SEC-MALS scheint eine polydisperse self-amplifying RNA (saRNA) eine gewichtsmittlere molare Masse, Mw, von 2 × 106 g/mol zu haben. FFF-MALS zeigt jedoch eine viel breitere Größenverteilung. Tatsächlich ist das wahre Mw um eine Größenordnung höher, und der Anteil des Materials, das mit SEC-MALS gesehen wird, macht lediglich <20 % der gesamten Probe aus.
Die ASTRA Number-Density-Methode bietet eine direkte Messung der Partikelgröße und -konzentration, die aus der Lichtstreuintensität abgeleitet wird. Diese Berechnungen können auf eine Vielzahl gängiger Gentransportvehikel angewendet werden, darunter Viren, virusähnliche Partikel und Lipid-Nanopartikel. Erfahren Sie mehr über die Empfindlichkeit und Linearität dieser Methode in der CDC-Veröffentlichung CDC: Quantitation of influenza virus using field flow fractionation and multi-angle light scattering for quantifying influenza A particles.
Die Lösungen von Wyatt zur Charakterisierung einer Vielzahl von Gentherapieprodukten werden in der Broschüre Characterization of Biologics and Complex Drugs beschrieben.
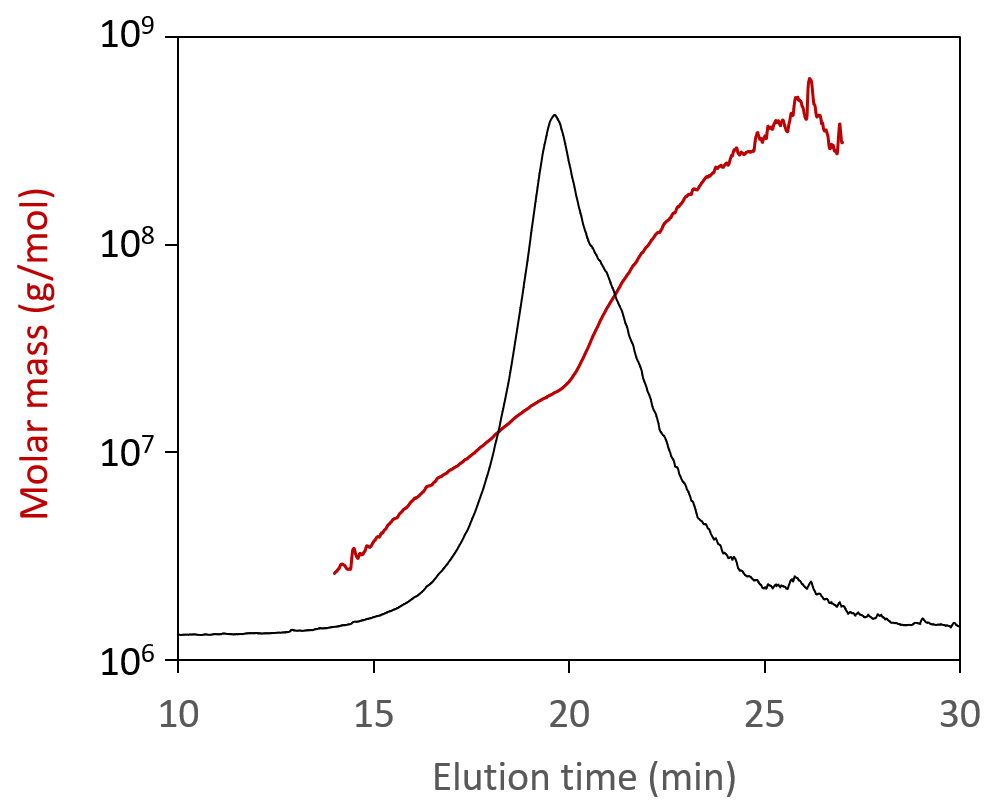
Molmassenwerte, gemessen für self-amplifying RNA (saRNA), überlagert mit dem FFF-MALS-Fraktogramm.
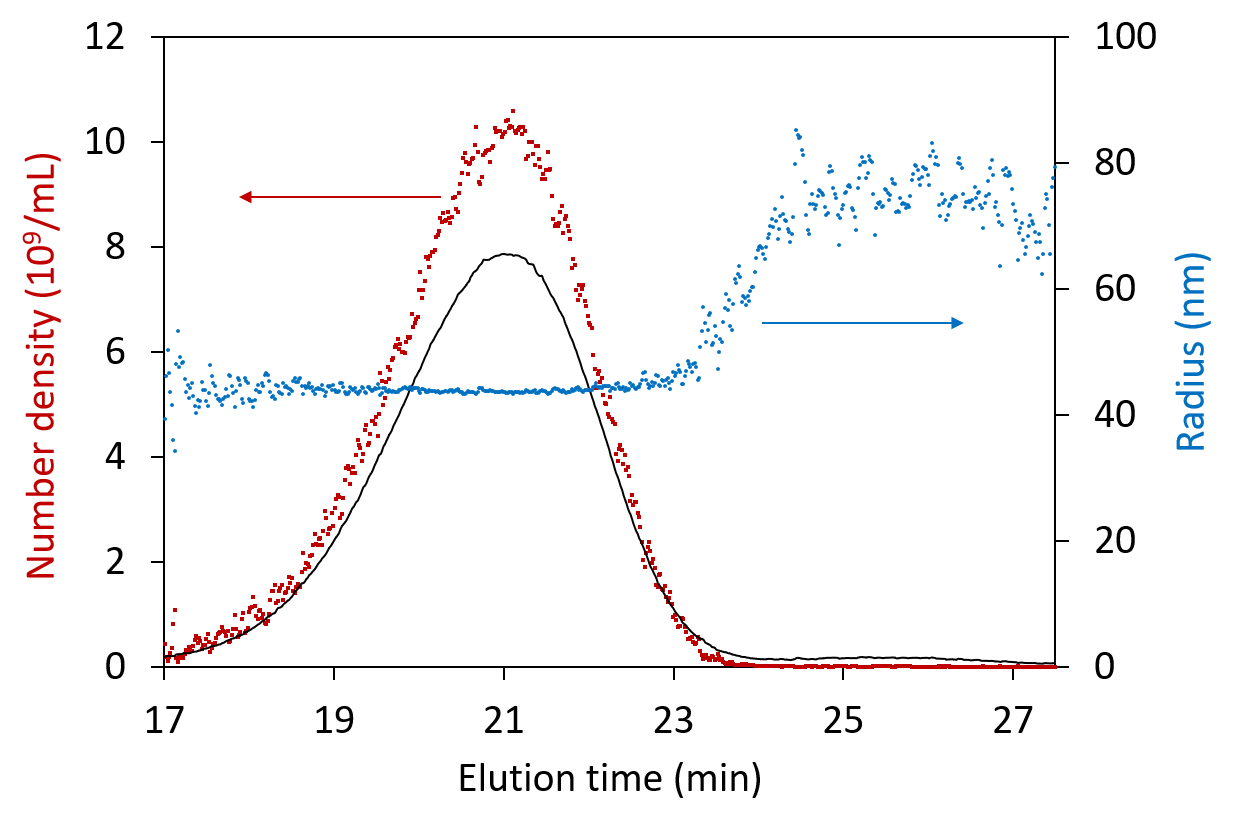
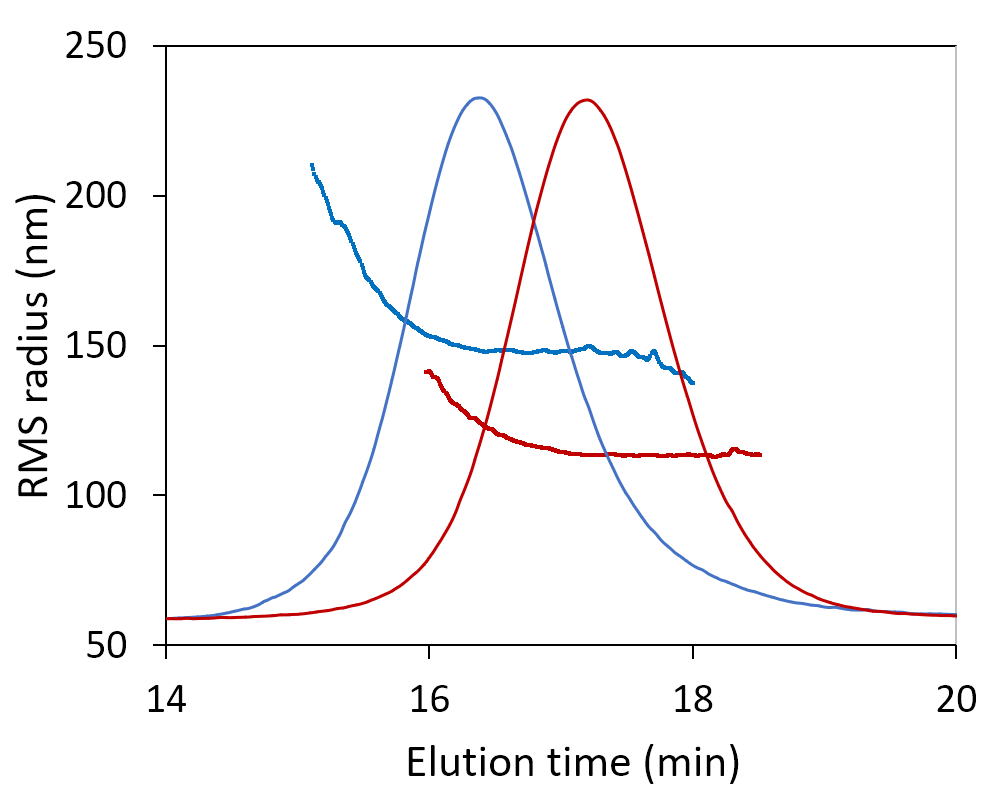
Analyse der Partikelkonzentration und des Partikelradius in jeder eluierenden Fraktion über den Peak, dargestellt für Viren, die mittels FFF getrennt wurden.
Orthogonale Quantifizierung von Aggregaten
Obwohl kleine Viren, wie AAVs, durch SEC-MALS gut charakterisiert werden, besteht die Möglichkeit, dass große Aggregate durch die Säule herausgefiltert werden. FFF-MALS ist eine ideale Technik, um diese Aggregate zu quantifizieren und eine orthogonale Charakterisierung zu liefern.
In diesem FFF-MALS-Fraktogramm sind die Aggregate deutlich von den monomeren und dimeren AAVs getrennt und eluieren bei ~25 Minuten Retentionszeit. Der mit FFF-MALS gemessene Größenbereich für den Peak umfasst Radien von ~20 nm bis ~100 nm, und der Peak enthielt 1.89 × 1014 Partikel, wie mit der ASTRA-Number-Density-Methode gemessen. Die überwiegende Mehrheit davon wurde jedoch durch SEC entfernt.
Erfahren Sie mehr über die FFF-MALS-Analyse von AAV-Aggregaten in unserer Application Note AN2003: Quantifying AAV aggregation and quality attributes by FFF-MALS.
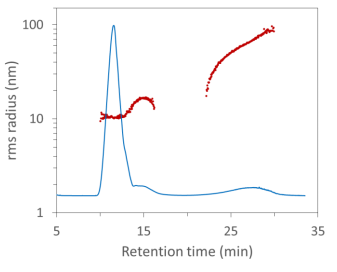
FFF-MALS-Analyse von AAV-Monomer, -Dimer und -Aggregaten, differenziert nach Radius. Die größeren Aggregate werden durch SEC herausgefiltert und sind daher nicht durch SEC-MALS quantifiziert.
AAV-Methode Implementierung & Schulung
Sensitive Messgeräte in Kombination mit leistungsstarken Softwarelösungen sind der Schlüssel zur Charakterisierung wichtiger Eigenschaften von Gentherapieprodukten. Um diese Werkzeuge optimal zu nutzen, benötigt es jedoch eine bewährte Methode. Diese Methode muss von der Entwicklung über den gesamten Produktlebenszyklus hinweg übertragbar sein.
Wyatt Technology bietet einen speziellen AAV-Methoden-Implementierungs- und Schulungsservice an, um Sie bei der Einführung der SEC-MALS-Viral Vector Analysis-Methode zu unterstützen. Im Rahmen dieses Service kommt ein Anwendungsspezialist mit einer schlüsselfertigen SEC-Methode und einer Standardarbeitsanweisung (SOP) zu Ihnen vor Ort, um sicherzustellen, dass Sie von Anfang an erfolgreich sind.
Die AAV-Methodenimplementierung & Training kann mit einer PM oder IQ/OQ vor Ort kombiniert werden, um sicherzustellen, dass Sie mit minimaler Ausfallzeit einsatzbereit sind. Eine unschätzbare Ressource für diese Methode ist das SOP Guidance Manual: Critical Quality Attributes of AAV by SEC-MALS, das als umfassendes Handbuch für die Anpassung einer Methode für den Einsatz in F&E, Produktion, QC und in Vergleichbarkeitsstudien dient.
