生物治疗药

开发高效、健壮的生物制剂是一个复杂的过程。光散射技术在每个阶段都有独特的多用途生物物理筛选和表征技术,从目标和候选发现到选择、优化、纯化、配方和制造规模扩大
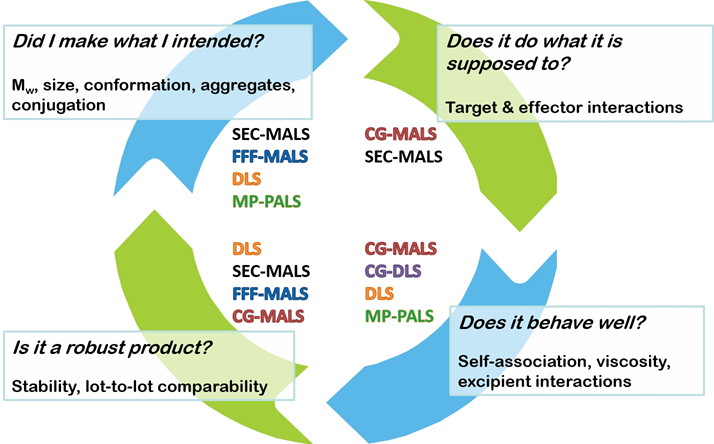
下面介绍光散射在生物治疗发展中的一些关键应用。
靶蛋白和候选蛋白
一旦确定了特定适应症的靶蛋白和候选生物分子,就必须以小规模生产足够数量和适当质量的蛋白质和候选生物分子,以便进行进一步的研发。
可溶性团聚体
具有多角度光散射(SEC-MALS)的尺寸排阻色谱法能够准确地表征蛋白质和其他生物分子的可溶性聚集体,而不考虑非理想的柱间相互作用,以快速确定最佳纯化条件。
稳定性
使用DynaPro®平板阅读器的高通量动态光散射(DLS)需要最少的样品数量和时间来评估候选样品和预配方条件,以确保稳定性和聚集性。
相互作用
成分梯度,多角度光散射(CG-MALS)结合Calypso成分梯度系统和DAWN®MALS检测器确定药物靶点结合的亲和力和绝对化学计量,无需标记或固定。它特别适合于研究多价相互作用或存在自缔合的药物靶点结合,包括病毒样颗粒(VLPs)、单体抗体、寡核苷酸或肽。
候选人选择与优化
翻译后修饰如糖基化或聚乙二醇化通常应用于蛋白质或肽,以提高稳定性和增加生理保留时间。一些生物制剂,如胰岛素,由于同样的原因,需要形成明确的低聚物状态。用共轭高毒性药物修饰IgG可以将抗体转化为有效的抗癌物质。
药物抗体比
三重检测SEC-MALS利用UV、MALS和RI联合检测仪,可方便地测定糖基化或聚乙二醇化程度,在许多情况下可用于计算抗体-药物结合物(ADC)的药物抗体比(DAR)。
齐聚
CG-MALS通过测量重量平均摩尔质量与浓度的关系来分析可逆齐聚反应。寡聚物的顺序可以与亲和力一起明确地确定。
抗体工程和通过基因序列突变进行的其他修改可用于提高稳定性或疗效。SEC-MALS有助于确定这些更改对聚合的影响,而CG-MALS则评估它们如何影响目标绑定属性。
生物类
对于更大的实体,如病毒样颗粒(VLPs)和聚合物、脂质体或水凝胶基药物载体,通过场流分馏(FFF)分离通常比大小排阻色谱更可取。Eclipse™DualTec™和Eclipse AF4 FFF系统为MALS探测器上游的最佳分离提供了多种选择。
过程开发
光散射测量有助于以多种方式进行过程开发:
净化终点
由于多角度光散射独立于保留时间确定摩尔质量,因此RT-MALS是实时表征纯化产物和测定终点的理想方法。为了在工艺开发过程中更详细地描述产品特性,SEC-MALS可与UHPLC一起实现快速分离和分析。
第四纪构造
复杂产品,如病毒样颗粒或肽胶束,必须具有特定的质量、形状和大小,以及最小数量的剩余未组装材料。SEC-MAL或带在线DLS的FFF-MAL验证这些过程,以量化未装配的子单元,并确保最终产品符合要求的结构。
配方
在配方过程中,缓冲条件和赋形剂的许多组合必须进行稳定性和聚集性测试。最终选择最有希望的长期试验条件并不一定需要严格的热力学特性,但有助于理解反映稳定性各个方面的多种特性。高通量DLS是实现这一目标的理想技术,因为它可以处理多个稳定指示参数,同时每天测试数千个条件:
稳定性筛选
- 聚集状态 - 聚集物的形成、粒度分布和形成速率。这是基本的DLS分析。
- 热稳定性 - 温度如何导致变性和非自然聚集。通过温度梯度测定,监测分子大小的变化。
- 化学稳定性 - 缓冲成分(pH、离子强度、变性溶剂如胍)如何引起变性和非自然聚集。通过组成步骤测定,监测分子大小的变化。
- 胶体稳定性 - 表面部分如带电残基或疏水斑块如何导致聚集,与三级结构的变化无关。通过平移扩散的浓度依赖性,kD或D1来确定。
使用DynaPro平板阅读器,这些测量在标准96、384或1536微孔板上进行,消耗的样品量最少。同样的样品可在相同或其他基于板的仪器中进一步测试[例如,分析胶体稳定性(在DynaPro中)或固有荧光(在光谱板读取器中)的温度依赖性],使DynaPro板读取器成为配方筛选的宝贵工具。一个软件包可以将仪器与机器人样品制备和平板放置集成在一起。
分子电荷
另一个有助于配方开发的光散射工具是电泳光散射(ELS)。Mobius™与自动进样器和阿特拉斯集成,用于自动测量分子电荷,这是稳定性的一个重要参数。即使在中等至高盐条件下,测量也在本机缓冲区中进行。与DynaPro®读板器一样,Mobius提供了多种参数的自动测量,如热稳定性和胶体稳定性。
浊度
浊度意味着溶液中聚集和颗粒的形成、出现可逆自缔合(RSA)或液-液相分离,导致不良产品性能。具有微升级进样体积的DynaPro® NanoStar®可快速测量配方的浊度。
高浓度配方
在高浓度单克隆抗体和其他生物治疗药物的制备过程中,额外的表征挑战包括理解弱相互作用和粘度的相互作用。
蛋白质-蛋白质相互作用
在低浓度下,弱蛋白-蛋白质相互作用可能不重要,因此不一定反映在稀释条件参数(如kD)中,但在高浓度下,弱蛋白-蛋白质相互作用占主导地位。CG-MALS通过一个称为Minton-Chatelier形式主义的理论框架独特地解决了这些复杂的相互作用。这项技术区分了引起聚集和粘性的吸引相互作用和可能影响测量但对稳定性影响不大的排斥相互作用。
粘度筛选
粘度既是胶体稳定性的标志,也是一个重要的参数,因为高粘度影响最终产品的可制造性和可交付性。DLS可利用示踪珠测定浓缩蛋白溶液的粘度。DynaPro平板阅读器可以在几秒钟内评估小到10微升的样品粘度,每天测量数千个条件,以便筛选出理想的降粘辅料。
浊度的测量
在高浓度配方中,由于溶液中不同物质之间的相互作用会导致乳光和产品质量差,因此浊度的测量变得至关重要。溶液的浊度由浊度校准图(turbidity calibration plot)测定。 石英比色杯根据一系列浊度标准进行校准,随后在该比色杯中溶液的浊度测量结果被计算并以浊度单位 (NTU) 显示在数据表中。访问浊度页面了解更多信息。
生物物理特性
光散射是任何生物治疗生物物理特性实验室的重要组成部分,被FDA认定为监管备案的关键技术。关键应用包括:
聚合
应用基于光散射和怀亚特公司提供的其他仪器的正交技术,分析支持实验室可以通过对可溶性和不溶性亚微米聚集体的彻底验证和扩展分析来支持监管文件。这些技术包括:
- SEC-MALS用于可溶性不可逆聚集体质量和尺寸分布的稳健表征
- 用于稳健表征的FFF-MALS可溶性和不溶性、不可逆聚集体的质量和尺寸分布
- 快速测定可溶性和不溶性、可逆和不可逆集料粒度分布的批处理DLS
- 用于表征可逆聚集体或低聚物的CG-MALS,以及验证SEC-MALS在色谱柱上的聚集体损失。
共轭
通过紫外线-MALS-dRI进行三次检测,确定以下物质的组成和摩尔质量分布:
- 蛋白多糖结合疫苗
- 聚乙二醇化蛋白质
- 抗体药物结合物
- 糖蛋白类
- DNA/RNA有效载荷的VLPs
通过添加WyattQELS DLS模块,还可以确定尺寸分布。
- 化学处置: 电致发光决定电荷状态,是表面化学的重要指标。
- 功能性: CG-MALS是一种无需标记或固定化,可深入表征药物-靶点结合等生物分子相互作用的有力技术。由于它直接测量摩尔质量,它特别适用于一系列价态和自缔合以及杂缔合。
疫苗
不同种类疫苗中使用的成分种类繁多,因此很难总结光散射应用于疫苗研制的所有方法。以下是一些:
多糖疫苗
多糖往往是非常不均匀的;感兴趣的性质包括摩尔质量和大小的分布以及构象。在大多数情况下,SEC-MALS与联机DLS结合提供了良好的分辨率和完整的信息。当多糖摩尔质量很高且分子高度分枝时,由于FFF中不存在导致SEC异常分离的锚定效应,FFF-MALS-DLS将提供更好的数据。
蛋白质-多糖结合物
SEC柱校准不能用于表征蛋白质-多糖缀合物的分子量,因为不存在相关标准。只有采用三重检测技术(UV-MALS-RI)和“共轭分析”算法的SEC-MALS才能提供准确可靠的摩尔质量分析,不仅提供总分子量,还提供组成蛋白质和多糖的质量。即使复合物中含有额外的成分,如脂质,也可以测定蛋白质和总摩尔质量。
同样的分析也适用于FFF分离。
病毒和病毒样颗粒(VLP)
光散射耦合FFF法是一种较简便的病毒粒子计数方法,其结果与低温TEM法非常相似。
DLS、SEC-MALS和FFF-MALS在VLP的开发和生产过程中广泛使用:
- SEC-MALS用于评估将盖小体组装成良构VPS以及VLP分子量、大小、聚集状态、形状和均匀有效载荷
- 当VLP不能很好地从SEC柱中洗脱时,用于相同特征的FFF-MALS
- 用于高通量配方的DLS
脂质体
脂质体可作为抗原的载体和佐剂。DLS是一种快速测定脂质体大小的良好方法。当需要更精确的分布或附加特征(如形状或有效载荷)时,SEC-MALS和FFF-MALS提供了具有优异分辨率的可靠结果。
抗体相互作用
需要评估抗体与分离抗原蛋白或复合疫苗(如VLP)结合的程度?CG-MALS测定溶液中的结合亲和力和绝对分子化学计量学,无需标记。它在评估包含多个抗原的多价疫苗中的蛋白质-蛋白质相互作用方面也是非常有价值的。
在目前的生物治疗生产策略中,“过程就是产品”是指严格控制pH、温度、原料消耗等工艺参数,以保证产品质量。只有在过程结束时,QC程序才能检查定义产品质量的关键质量属性(cqa)。因此,大多数PAT仪器监测的是工艺条件,而不是产品属性。

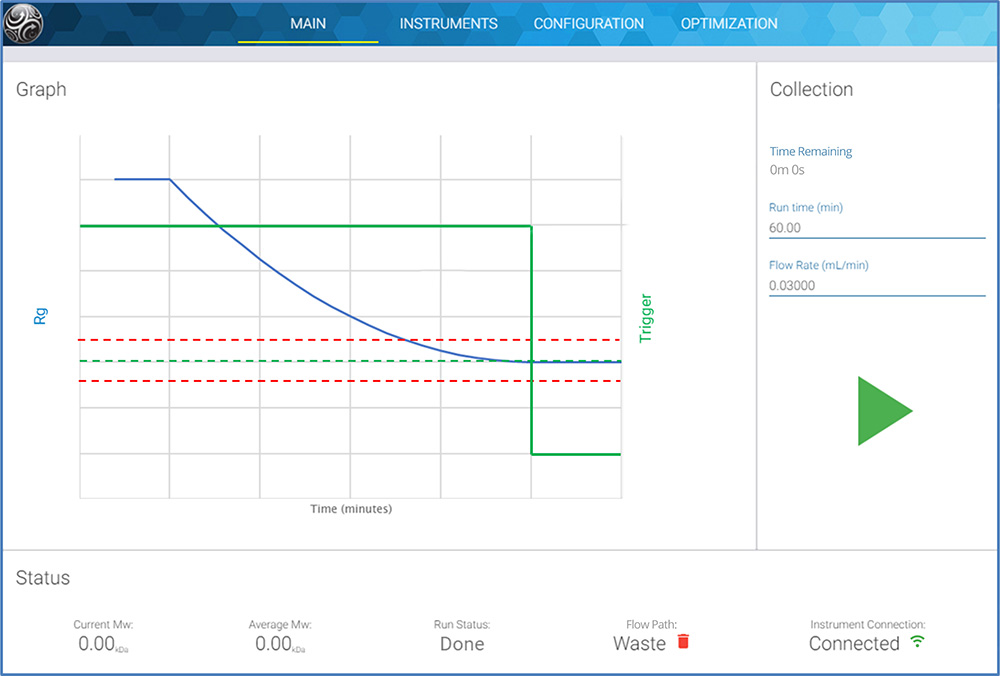
实时多角度光散射(RT-MALS)是光散射的一种新的PAT应用,它直接决定了mAbs等治疗性生物分子的分子量。它对骨料和污染物颗粒的外观特别敏感。使用ultraDAWN™RT-MALS仪器,在线或在线净化和其他工艺步骤,生产人员可以加快和优化工艺开发,并立即反馈工艺变化和偏差的影响。对于直径在25-30nm以上的病毒样颗粒和其他生物分子复合物,ultraDAWN测量的是另一个属性,即平均半径。
在开发了这个过程之后,超黎明号可能会留在网上。其配套软件OBSERVER™与OPC-UA环境集成,实现自动化和/或GMP操作。可编程观测器,以触发系统对因聚集而偏离允许摩尔质量范围的反应,或在达到终点后停止反应。
部分文献
Esfandiary, R.; Hayes, D. B.; Parupudi, A.; Casas-Finet, J.; Bai, S.; Samra, H. S.; Shah, A. U.; Sathish, H. A. A systematic multitechnique approach for detection and characterization of reversible self-association during formulation development of therapeutic antibodies. J. Pharm. Sci. 2013, 102, 3089-3099.
Lehermayr, C.; Mahler, H.-C.; Mäder, K.; Fischer, S. Assessment of net charge and protein-protein interactions of different monoclonal antibodies. J. Pharm. Sci. 2011, 100, 2551-2562.
Menzen, T.; Friess, W. Temperature-ramped studies on the aggregation, unfolding, and interaction of a therapeutic monoclonal antibody. J. Pharm. Sci. 2014, 103, 445-455.
Mohr, J.; Chuan, Y. P.; Wu, Y.; Lua, L. H. L.; Middelberg, A. P. J. Virus-like particle formulation optimization by miniaturized high-throughput screening. Methods 2013, 60, 248-256.
Rathore, A.; Krull, I. S.; Kreimer, S. The Use of Light-Scattering Detection with SEC and HPLC for Protein and Antibody Studies, Part I: Background, Theory, and Potential Uses. LCGC North America 2012, 30(9).
Rathore, A.; Krull, I. S.; Kreimer, S., Champagne, J. The Use of Light-Scattering Detection with SEC and HPLC for Protein and Antibody Studies, Part II: Examples and Comparison to Mass Spectrometry. LCGC North America 2012, 30(12).
Saito, S.; Hasegawa, J.; Kobayashi, N.; Tomitsuka, T.; Uchiyama, S.; Fukui, K. Effects of ionic strength and sugars on the aggregation propensity of monoclonal antibodies: influence of colloidal and conformational stabilities. Pharm. Res. 2013, 30, 1263-1280.
