纳米颗粒具有多样性且逐步在领域起到重要作用。表征它们首先需要克服以下难题,包括:
- 确定纳米药物(包括药物和基因传递载体)的大小、浓度、成分和构象
- 胶体悬浮液或纳米乳剂在控制释放应用中的稳定性评估
- 检测和识别可能渗入环境的少量工业添加剂
- 分析在食品、化妆品、半导体加工等消费品或工业产品中使用的纳米颗粒、乳剂和胶体的大小分布、ζ电位和在溶液条件(包括pH和离子强度)下的聚集行为
Wyatt的光散射工具包提供了纳米颗粒的基本分析仪器,具有无与伦比的自动化水平、灵敏度和分辨率。通过将通常使用的低通量手动测量转化为自动化的高通量工作流程,为在这一领域工作的科学家和工程师开辟了许多新的可能性。
在Wyatt仪器中应用于纳米颗粒和胶体表征的测量技术包括动态光散射(DLS)、多角度静态光散射(MALS)、场流分离(FFF)和电泳光散射(ELS)。
性质
尺寸分布
尺寸分布
动态光散射(DLS)是一种常见的方法,用于估计纳米颗粒和其他胶体悬浮液的大小,甚至在各种溶剂中以相对较短的时间内获得大致的尺寸分布。
然而,大多数DLS仪器需要手动将样品装入比色杯中,将比色杯插入仪器,操作软件开始数据收集,然后清洗比色杯,并重复整个过程以处理下一个样品 - 这是一个缓慢而费时的过程。Wyatt提供了两种自动化DLS的方法,使您可以设置并同时处理数十甚至数百个样品,从而解放您的时间,提高生产效率数十倍。
- DynaPro® Plate Reader在标准微孔板中执行DLS测量,包含96、384甚至1536个样品,每天可以完成数百甚至数千个样品。
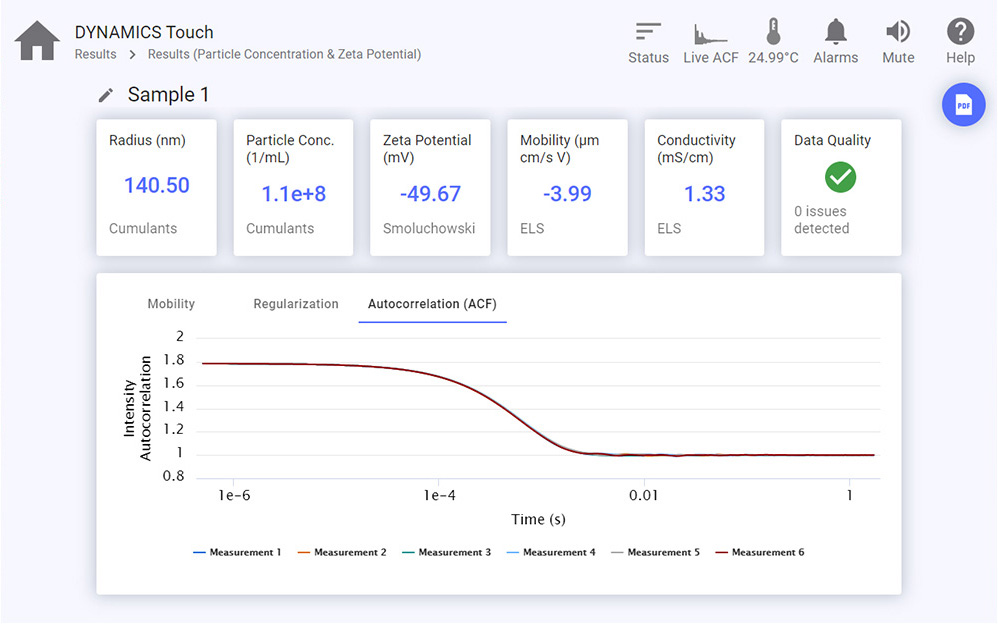
- ZetaStar™结合了同时进行DLS和电泳迁移率测量以确定大小和ζ电位的功能,可以连接到标准的自动进样器和高效液相色谱泵,以自动处理数十个大小和ζ电位测量实验。ZetaStar同时适用于有机和水性溶剂。
- 如果不需要自动化,DynaPro® NanoStar®提供了在非常宽的温度范围内进行基于比色杯的DLS测量,样品体积可以小至2微升。
在需要准确、高分辨率的纳米颗粒悬浮液大小分布的情况下,首选的分析工具是使用Eclipse™ FFF系统的场流分离(FFF),配备可选的集成WyattQELS™ DLS 模块的DAWN® MALS检测器。NanoStar也可以与Wyatt MALS检测器一起提供在线DLS检测,然后轻松切换回基于比色杯的DLS。
FFF在概念上与尺寸排除色谱有关,但在分离性能上远远超过SEC,拥有1-1000纳米范围,并具有出色的分辨率。而DLS充其量只能区分尺寸相差3-5倍的颗粒,FFF-MALS和FFF-DLS可以准确地表征尺寸相差仅几个百分点的颗粒。
颗粒浓度
颗粒浓度
光散射技术可以有效确定颗粒浓度(每毫升颗粒数量)和定量颗粒尺寸分布的方法。其中一种相对简单、快速和有效的选项是单机DLS结合多角度静态光散射(SLS)来进行,该技术在样品主要包含一个或两个具有明显大小的颗粒群,且颗粒半径不超过约160-225纳米的情况下最为准确。NanoStar、ZetaStar和DynaPro Plate Reader能够以这种方式确定颗粒浓度。
一种更为可靠和多功能的确定颗粒浓度的方法是FFF-MALS,它将基于大小的分离步骤与MALS检测和分析结合在一起。通过了解颗粒材料的折射率,MALS确定了每个洗脱大小分数中的纳米颗粒数量。FFF-MALS分析病毒、脂质体、脂质纳米颗粒、乳胶颗粒、细胞外囊泡和其他纳米颗粒的浓度和定量尺寸分布,其结果与透射电镜计数相似,误差在几个百分点内。FFF-MALS的颗粒浓度与颗粒追踪分析(particle tracking analysis)相比,覆盖了更大的尺寸范围,并且无需将样品稀释到指定的浓度范围内。
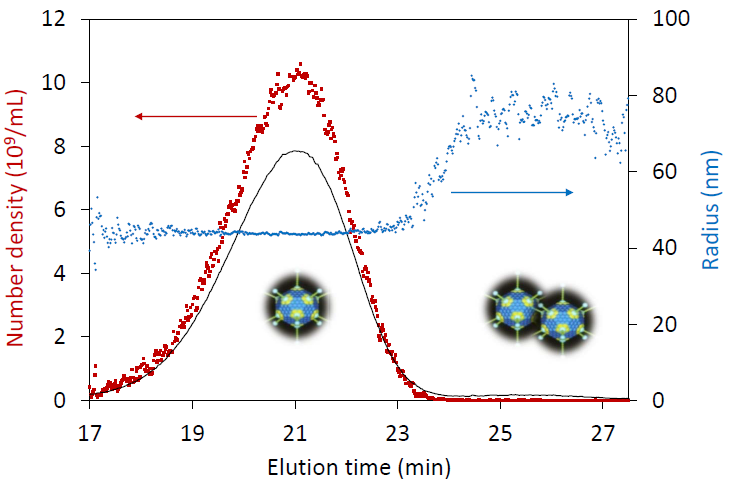
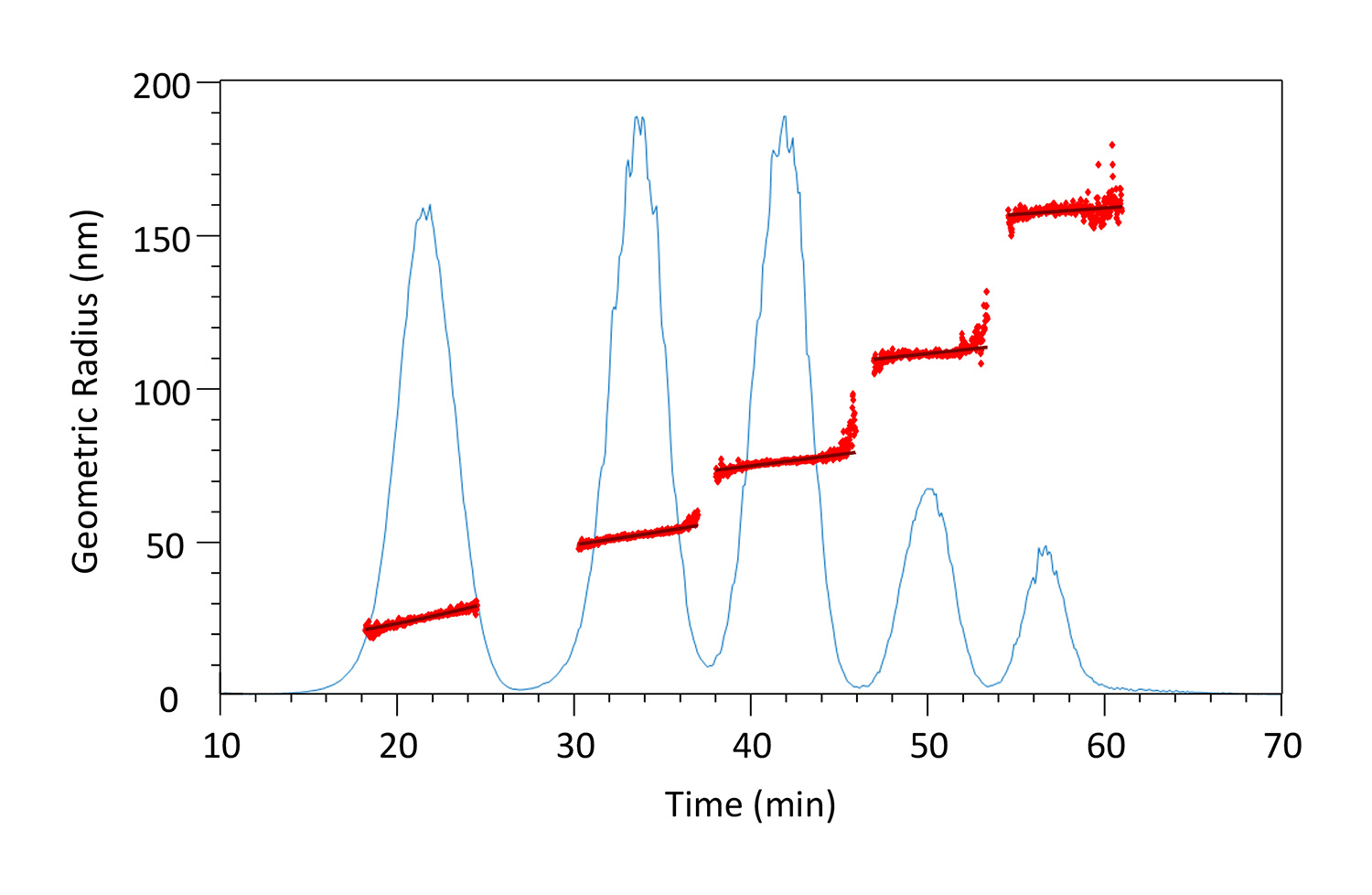
通过 FFF-MALS 分析每个洗脱组分的腺病毒大小和颗粒浓度。

FFF-MALS 系统包括 Eclipse FFF 控制器和流道、DAWN MALS 、Optilab dRI 以及泵、自动进样器和 UV 检测器。
构象
构象
尽管光散射技术不能提供纳米颗粒的高分辨率图像,但它是了解颗粒集合中形状或其他构象特性分布的有效手段。为了实现这一目标,使用了三种设备:Eclipse FFF分离系统、DAWN MALS检测器以及集成在DAWN中的WyattQELS DLS模块。
FFF通过尺寸分离颗粒。随着每个洗脱组分进入DAWN,光散射通过MALS进行rms半径Rg的独立测量,通过DLS进行流体动力学半径Rh的测量。Rg:Rh的比值,称为“形状因子”,提供了主要结构的预期值。
为了正确解释形状因子,需要一些有关预期形状的先验信息。如果已知颗粒是椭圆形且成分均匀,则形状因子表示偏离球形度和轴比的程度。如果颗粒已知是球形但可能是中空壳体或均匀球体,形状因子表示实际的构象,类似地,对于各种简单而明确定义的结构也是如此。
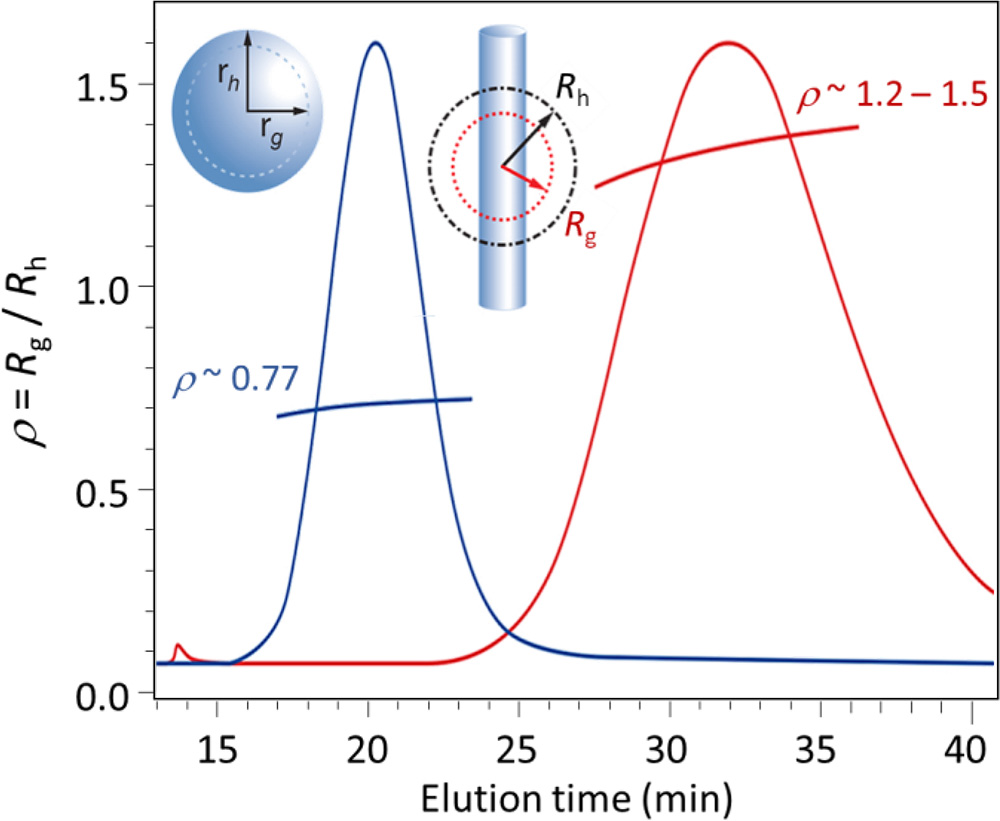
两种颗粒的 FFF-MALS-DLS 形状因子分析:球形(预期值 = 0.77)和棒状(预期值 > 1.1)。
构成
构成
FFF-MALS/DLS系统与ICP-MS耦合可以进行元素分析。在这种方法中,洗脱颗粒的大小和相对分布与质谱确认的元素组成相关联。这种联合技术已用于检查食物中发现的纳米颗粒的大小和化学组成,以及从湖泊和河流等自然来源中回收的纳米颗粒分数所关联的金属类型。
纳米药物递送颗粒(如脂质纳米颗粒、脂质体或PLGA)的有效荷载量可以通过SEC-MALS或FFF-MALS结合UV和RI检测来确定。这里提供了一个控释药物传递部分的示例。
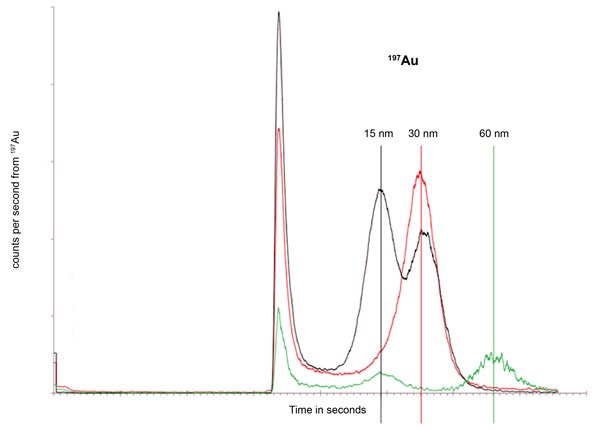
不同大小颗粒的金含量。 尺寸由 ICP-MS 系统上游的在线 DLS 确定。
技术与资源
过程分析技术
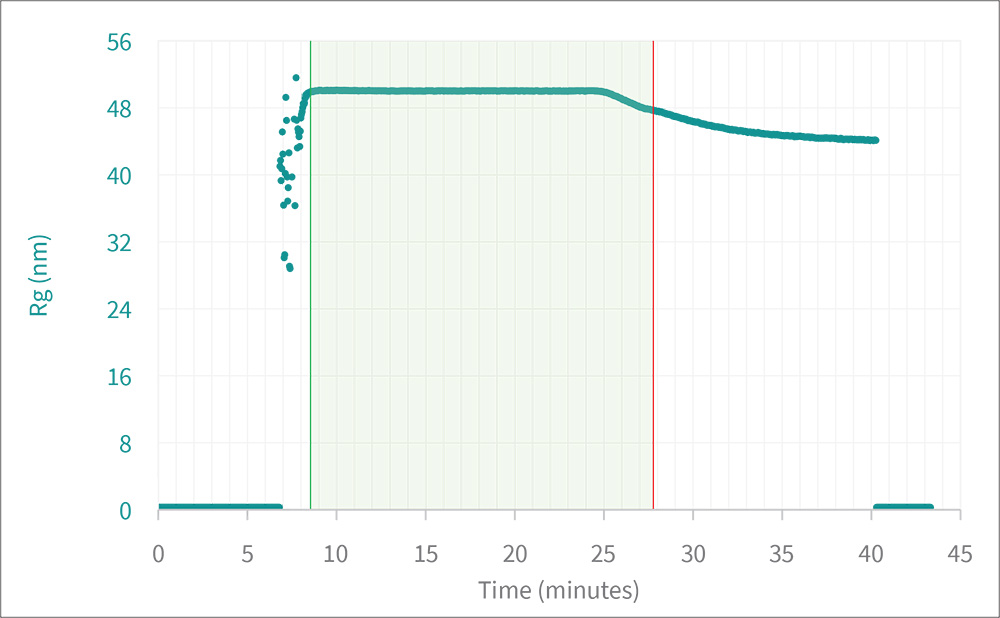
实时多角度光散射(RT-MALS)是脂质纳米颗粒、病毒、聚合物胶束和其他纳米颗粒的制造过程中进行分析的新技术。在制造过程中,大多数PAT仪器主要监测诸如pH、温度、压力和原料消耗等过程条件。仅在过程结束后,质量控制(QC)程序才能检查定义产品质量的实际物理属性。而有了RT-MALS,这种情况不再存在。
实时多角度光散射(RT-MALS)是光散射技术的一种新型PAT应用,直接确定直径在25到500纳米之间的纳米颗粒的大小和浓度。使用ultraDAWN™ RT-MALS仪器,可以在线或在线连接到生产、纯化和其他工艺步骤,制造人员可以通过对工艺变化和偏差的即时反馈,加速和优化工艺开发。
在开发完工艺后,ultraDAWN可以保持在线。其附带的OBSERVER™软件与OPC-UA环境集成,实现自动化和GMP操作。OBSERVER可以编程,触发系统对由于工艺波动导致的尺寸偏差做出反应,或在达到终点时关闭反应。

制剂
制剂
在多种溶剂条件下,对纳米颗粒的聚集和稳定性进行高通量筛选对于高效的制剂工作至关重要。DynaPro Plate Reader是于制剂契合度极高的工具,它可以在标准微孔板中对数百个样品进行DLS筛选,评估大小、多分散性和聚集,而且是在全自动测量。DynaPro可以轻松与液体处理机器人联用,提高生产效率。
如果不需要高通量,基于比色杯的DynaPro NanoStar是一款多功能仪器,可以与Wyatt MALS联用,提供在线DLS(例如FFF-DLS)。
除了用于大小、摩尔质量、热稳定性和胶体稳定性的DLS/SLS外,ZetaStar结合了同时进行DLS和ELS以进行大小和ζ电位测定。独特的是,在ZetaStar中,ζ电位测量可以手动进行,也可以通过使用流通池的自动进样器自动进行。Atlas™配件增加了ZetaStar的实用性,使其能够在高离子强度条件下进行测量。与NanoStar类似,ZetaStar还可以与Wyatt MALS仪器耦合,进行在线DLS测量。
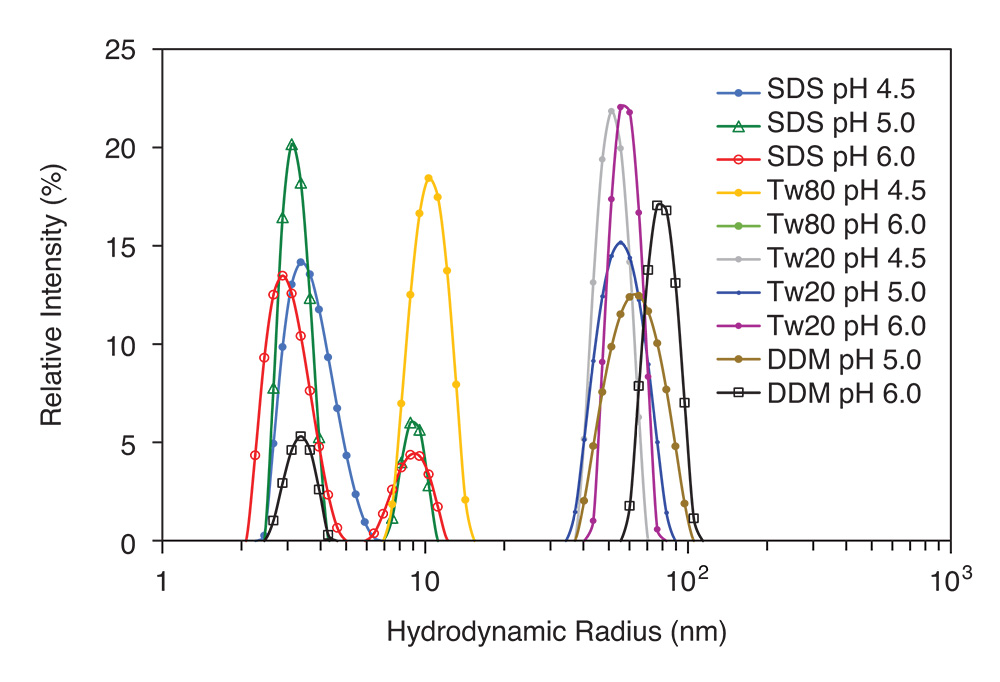
使用DynaPro Plate Reader通过 DLS 自动筛选数十或数百种纳米颗粒制剂的尺寸。
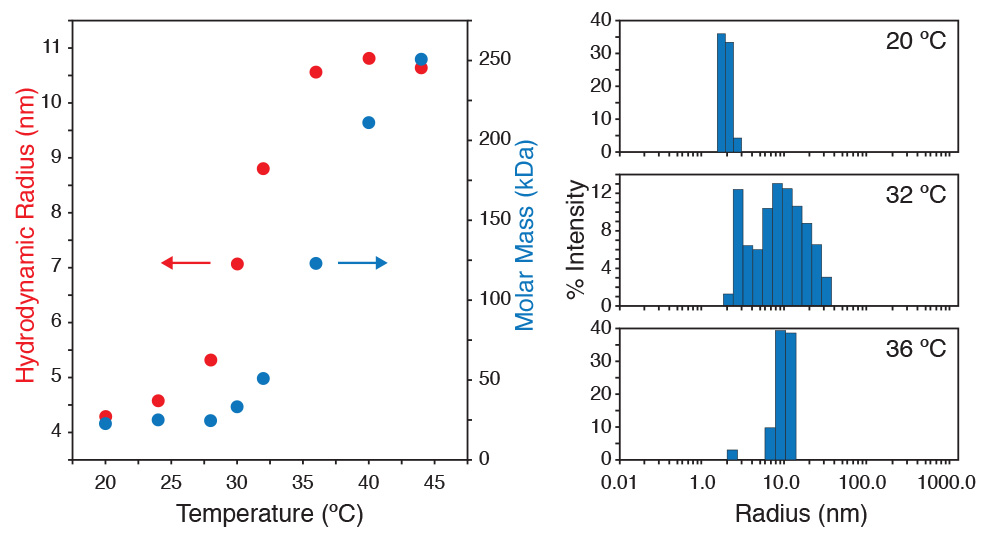
在基于DynaPro NanoStar比色杯的 DLS 仪器中同时进行静态和动态光散射测量,揭示了聚合物囊泡的临界胶束温度。 NanoStar 还与 DAWN MALS 仪器进行光学联用,用作在线 DLS 检测器。
纳米制剂和药物递送
纳米制剂和药物递送
光散射和场流分离提供了开发新型纳米制剂所必需的表征能力,无论是携带 RNA 的脂质纳米颗粒、携带药物的脂质体,还是 PLGA 胶束等其他载体。
通常,对纳米制剂颗粒的基本尺寸测量最初在单机(未分离)的动态光散射(DLS)仪器中进行,该仪器在比色杯中进行测量,例如DynaPro NanoStar或ZetaStar。更准确的大小分布可以通过分离步骤来获得,例如对于直径约为100纳米的颗粒可以使用SEC-MALS,对于直径为1000纳米的颗粒可以使用FFF-MALS。这两种技术足够灵敏,可以解析在异质分布中半径相差几纳米的颗粒。
在纳米制剂开发中最重要的分析挑战之一是确定药物、治疗性肽或核酸是否进入载体中、结合在外部还是与没有进入载体。将SEC或FFF与DAWN MALS检测器和WyattQELS online DLS模块相结合,可以通过识别颗粒的构象和大小相关的成分,以及检测和识别未结合分子,来帮助回答这些问题。
对于稳定的制剂,纳米制剂构造物可以在DynaPro Plate Reader中在数十甚至数百种条件下评估,以最大限度地减少聚集。ZetaStar非常适合在一系列制剂缓冲液中测量药物递送纳米颗粒的ζ电位,以及在高盐缓冲液中进行测量。当电解形成电极上的气泡时,传统的ζ电位测量会受到干扰,而采用全新技术的ZetaStar不受受到干扰。ζ电位是N/P比和胶体稳定性的重要指标。
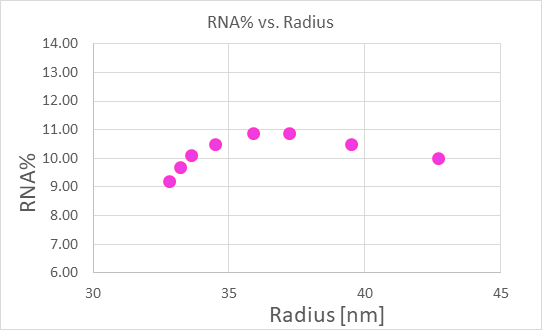
使用 FFF-MALS-UV-dRI 获得的 LNP-mRNA 制剂中 RNA含量与尺寸之间的纳米共轭分析。
应用文摘
精选文献
Selected references
Afonin, K. A.; Kasprzak, W.; Bindewald, E.; Puppala, P. S.; Diehl, A. R.; Hall, K. T.; Kim, T. J.; Zimmermann, M. T.; Jernigan, R. L.; Jaeger, L.; Shapiro, B. A. Computational and experimental characterization of RNA cubic nanoscaffolds. Methods 2014, 67, 256-265.
Dhayal, S. K.; Gruppen, H.; de Vries, R.; Wierenga, P. A. Controlled formation of protein nanoparticles by enzymatic cross-linking of α-lactalbumin with horseradish peroxidase. Food Hydrocolloid. 2014, 36, 53-59.
Loeschner, K.; Navratilova, J.; Legros, S.; Wagner, S.; Grombe, R.; Snell, J.; von der Kammer, F.; Larsen, E. H. Optimization and evaluation of asymmetric flow field-flow fractionation of silver nanoparticles. J. Chromatogr. A 2013, 1272, 116-125.
Perevyazko, I. Y.; Delaney, J. T.; Vollrath, A.; Pavlov, G. M.; Schubert, S.; Schubert, U. S. Examination and optimization of the self-assembly of biocompatible, polymeric nanoparticles by high-throughput nanoprecipitation. Soft Matter 2011, 7, 5030-5035.
Wyatt, P. Submicrometer particle sizing by multiangle light scattering following fractionation. J. Colloid Interf. Sci. 1998, 197, 9-20.